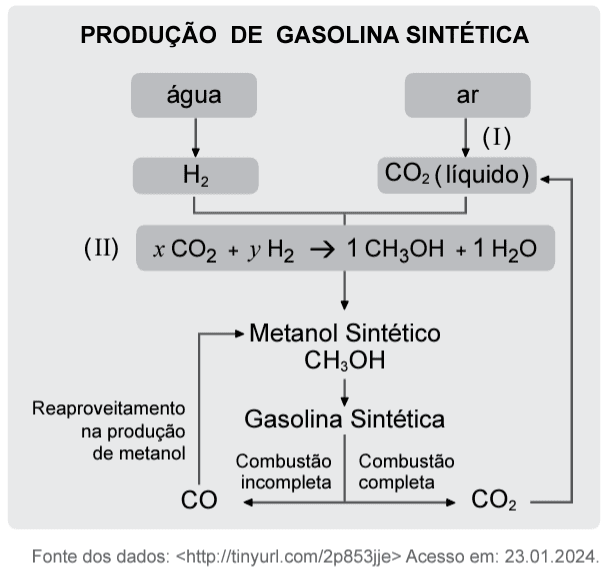
No extremo sul do Chile, foi inaugurada, em 2022, a primeira planta industrial do mundo para produção de combustíveis ecológicos. O processo utiliza dois recursos: o vento e a água, que são abundantes na região. O vento é responsável pela geração de energia elétrica limpa fornecida à usina. Essa energia é utilizada a fim de realizar a eletrólise da água para obtenção de hidrogênio, substância usada na produção do combustível sintético (denominado e-fuel). Uma estação aspira o ar atmosférico e separa o dióxido de carbono dos demais componentes do ar. Por meio de pressurizadores, condensadores e filtros, o CO2 é armazenado no estado líquido. Feito isso, o próximo passo é reagir o CO2 com o hidrogênio, gerando o metanol sintético que, refinado, resulta na gasolina sintética, conforme o esquema.
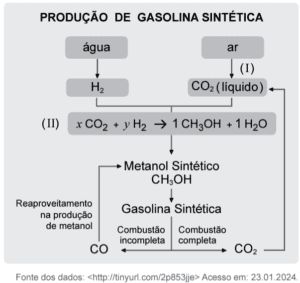
Considerando a equação química (II), que representa a reação de produção de metanol, os valores de x e y, que tornam a equação corretamente balanceada, são, respectivamente,
(A) 1 e 1.
(B) 1 e 2.
(C) 1 e 3.
(D) 2 e 1.
(E) 2 e 3.
Solução:
Nós temos 1 carbono de cada lado e 2 oxigênios de cada lado, logo x = 1, para que mantenha essa igualdade.
Temos 2 hidrogênios do lado esquerdo e 6 hidrogênios do lado direito, logo y = 3 para que tenhamos 6 hidrogênios do lado esquerdo, mantendo a igualdade.
Resposta: letra C.

















0 comentários